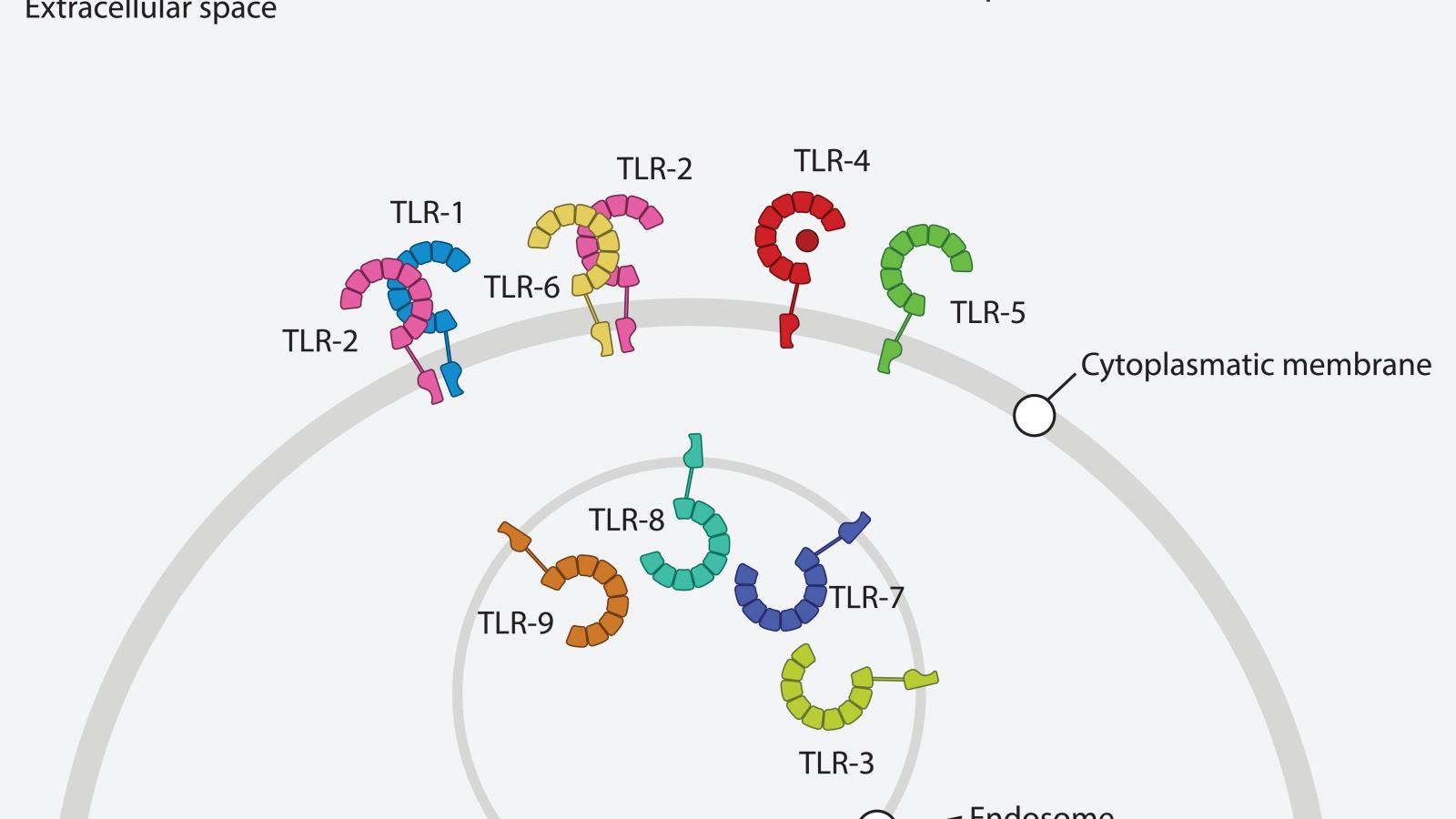
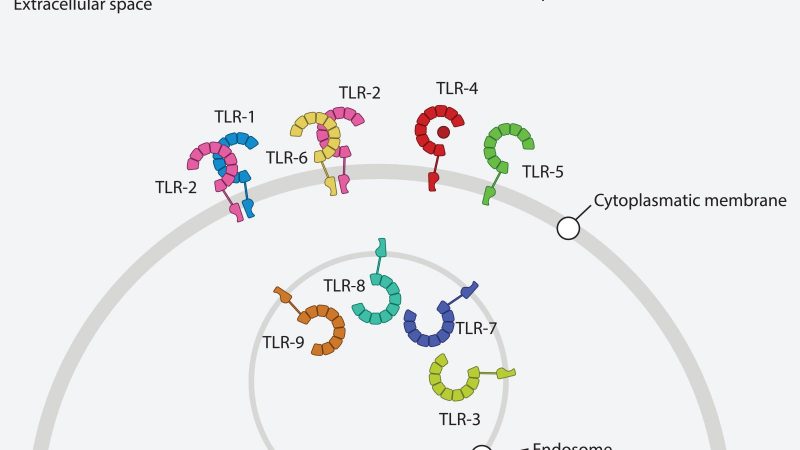
Una nueva revisión sobre los receptores tipo Toll (TLR) resume sistemáticamente cuarenta años de descubrimientos en el campo de los TLR, desde la identificación inicial de Toll en el desarrollo embrionario de la Drosophila hasta la comprensión actual de los mecanismos reguladores multicapa que gobiernan la señalización de los TLR.
La capacidad del sistema inmunitario innato para detectar patógenos mientras mantiene la autotolerancia ha sido una cuestión central en la inmunología. El descubrimiento de los receptores tipo Toll como receptores de reconocimiento de patrones que detectan patrones moleculares asociados a patógenos y a daños revolucionó este campo, lo que les valió el Premio Nobel de Fisiología o Medicina en 2011. Sin embargo, la investigación de la última década ha revelado que la señalización de los TLR es mucho más matizada de lo que se apreciaba inicialmente; el huésped ha desarrollado múltiples capas de mecanismos reguladores que operan en paralelo y en diafonía.
Las modificaciones postraduccionales como la fosforilación, la ubiquitinación, la metilación, la acetilación, la SUMOilación, la succinilación y la nitrosilación, cada una de ellas ajustando la intensidad de activación de los TLR y la duración de la señal. Los mecanismos epigenéticos —incluida la metilación del ADN, las modificaciones de las histonas, la remodelación de la cromatina y las modificaciones del ARN— dan forma al panorama de la cromatina de las respuestas de los TLR en escalas de tiempo más largas. La reprogramación metabólica revela una diafonía bidireccional entre el metabolismo energético, la oxidación de ácidos grasos, el metabolismo de los lípidos, el metabolismo de los aminoácidos y la señalización de los TLR, formando bucles de retroalimentación flexibles.
De particular interés, la identificación de condensados biomoleculares impulsados por la separación de fases representa una dimensión completamente nueva de la regulación de los TLR, ofreciendo nuevas perspectivas sobre la dinámica espaciotemporal de la transducción de señales inmunitarias innatas.
La revisión delinea además cinco modos fundamentales de regulación cruzada que permiten la integración de señales: interacciones complejas entre múltiples modificaciones postraduccionales desencadenadas por el mismo estímulo patógeno; convergencia de modificaciones postraduccionales, regulación metabólica y modificaciones epigenéticas para formar un sistema de respuesta estable pero flexible; amplificación sinérgica cuando diferentes TLR son activados por ligandos distintos; regulación mutua entre los mecanismos efectores posteriores a diferentes TLR; y una extensa diafonía entre los TLR y otras vías de receptores de reconocimiento de patrones. En conjunto, estos mecanismos aseguran respuestas inmunitarias precisas y equilibradas.
Más allá de los eventos moleculares intracelulares, la señalización de los TLR está profundamente integrada con diversas señales extrínsecas del microambiente tisular. Las señales de muerte celular, las redes de citoquinas, los gradientes de oxígeno, la disponibilidad de nutrientes, la regulación neuroinmune, las fuerzas mecánicas y las fluctuaciones del pH se cruzan con la red de TLR para dar forma a la dirección de las respuestas inflamatorias. Esta capacidad integradora permite a los TLR generar resultados inmunitarios apropiados al contexto en una amplia gama de entornos fisiopatológicos, incluyendo infección, lesión tisular, autoinmunidad, cáncer y envejecimiento inflamatorio.
En paralelo, los patógenos han desarrollado sofisticadas estrategias de evasión, incluyendo el enmascaramiento de los PAMP, la degradación o el secuestro de las moléculas de señalización de los TLR, la explotación de la desregulación inmunitaria del huésped y la manipulación de los mecanismos de separación de fases. “Estas tácticas de evasión, a su vez, proporcionan anotaciones funcionales naturales de nodos críticos dentro de la vía de los TLR”, propusieron los autores.
La señalización aberrante de los TLR está estrechamente relacionada con múltiples enfermedades humanas. En enfermedades infecciosas, los polimorfismos de los TLR influyen significativamente en la susceptibilidad del huésped. En afecciones autoinmunes como el lupus eritematoso sistémico, la artritis reumatoide, la psoriasis y la enfermedad inflamatoria intestinal, la sobreactivación o desregulación de los TLR endosomales (TLR7, TLR8, TLR9) es un motor central de la patogénesis. En el cáncer, la señalización de los TLR exhibe una compleja dualidad, capaz tanto de activar la inmunidad antitumoral como de promover la iniciación y metástasis del tumor. En la inmunosenescencia y la inflamación asociada al envejecimiento (inflammaging), la señalización desregulada de los TLR sirve como un centro clave que conecta el envejecimiento con diversas enfermedades relacionadas con la edad. Estos profundos vínculos entre los mecanismos fundamentales y la patología humana subrayan el potencial terapéutico de dirigirse a las vías de los TLR.
Las estrategias farmacológicas dirigidas a los TLR están evolucionando rápidamente. Agentes aprobados como el MPLA, el imiquimod y el CpG-1018 han demostrado valor clínico como adyuvantes de vacunas o en la inmunoterapia tópica. Sin embargo, los agonistas sistémicos de los TLR se enfrentan a importantes obstáculos traslacionales, con fracasos en etapas avanzadas de compuestos como el eritoran y el PF-3512676 que destacan la necesidad de una sincronización precisa, la estratificación de pacientes y estrategias de administración optimizadas.
“Las futuras direcciones se están desplazando de la activación inmunitaria amplia a la modulación de precisión de la señalización específica de la enfermedad”, señalaron los autores, “incluyendo ligandos sesgados o moduladores alostéricos para la regulación dirigida a la vía, sistemas de administración inteligentes como nanopartículas para la precisión espaciotemporal, estratificación de pacientes impulsada por biomarcadores y la integración de las interacciones huésped-microbioma en el diseño terapéutico”.
La historia de la investigación de los TLR está lejos de terminar. Esta importante revisión no solo sintetiza las redes reguladoras intrínsecas, las interacciones del microambiente tisular y los diversos roles de la señalización de los TLR en las enfermedades, sino que también tiende un puente entre el conocimiento mecanicista establecido y las necesidades clínicas no cubiertas. Con los continuos avances en inmunología de sistemas, biología estructural, inteligencia artificial y tecnologías de administración de precisión, se espera que la modulación precisa de las vías de los TLR desempeñe un papel cada vez más importante en la inmunoterapia futura para enfermedades infecciosas, enfermedades autoinmunes, cáncer, neurodegeneración y rechazo de trasplantes.
Related Content
-
January 16, 2026
-
January 7, 2022
-
July 26, 2017
It's Monday morning and my first patient is a newly diagnosed rheumatoid. This is…
-
January 16, 2026
The year 2025 presented numerous advances in rheumatology and related inflammatory and autoimmune…
-
December 9, 2025
Other videos in the Advanced Practice Rheum Series:Evaluation of Rheumatic ComplaintsRheumatoid & Inflammation…
-
May 14, 2022
Anakinra in Pediatric, Adult Still's Disease: Dr. Bella Mehta https://youtu.be/hgL71GdcYiI Recognition and Early…